高松医生的科普号
- 精选 化疗止吐三大方案总结
本文为NCCN临床实践指南:止吐(2016.V2)完整翻译版。此部分较2015版更新较多,与2016V1版相比,本文翻译的部分只有2处为更新。高度致吐风险化疗药引起急性或迟发型呕吐的预防方案化疗前开始。第一天,A、B、C方案任选其一,无偏重,但若d1选择A方案,d2、3、4也要接着用A方案,以此类推。A方案(NK1受体拮抗剂+5HT3受体拮抗剂+类固醇激素)[1类推荐]d1:NK1受体拮抗剂(任选一种)阿瑞吡坦 125mg po qd福沙吡坦 150mg iv qd罗拉吡坦 180mg po qd5HT3受体拮抗剂(任选一种)多拉司琼 100mg po qd格拉司琼 ①2mg po qd ②0.01mg/kg(最大1mg) iv qd ③ 第一剂化疗药前 24-48h 使用皮肤贴剂(规格为3.1mg/24h)昂丹司琼 ①16-24mg po qd ②8-16mg iv qd帕洛诺司琼 0.25mg iv qd类固醇激素地塞米松 12mg po/iv qd若d1给予口服阿瑞吡坦:阿瑞吡坦 80mg po qd d2-3+地塞米松 8mg po/iv qd d2-4若d1给予福沙吡坦:d2-3不再使用NK1受体拮抗剂,但使用类固醇激素地塞米松8mg po/iv qd d2,然后地塞米松8mg po/iv bid d3-4若d1给予罗拉吡坦:d2-3不再使用NK1受体拮抗剂,但使用类固醇激素地塞米松8mg po/iv bid d2-4B.包含奈妥吡坦的方案d1:奈妥吡坦300mg/帕洛诺司琼 0.5mg po qd地塞米松 12mg po/iv qdd2-4:地塞米松8mg po/iv qdC.包含奥拉西泮的方案d1:奥拉西泮 10mg po qd帕洛诺司琼 0.25mg iv qd地塞米松 20mg iv qdd2-4:奥拉西泮 10mg po qd中度致吐风险化疗药引起急性或迟发型呕吐的预防方案化疗前开始。第一天,A、B、C方案任选其一,无偏重,但若d1选择A方案,d2、3、4也要接着用A方案,以此类推。A方案(5HT3受体拮抗剂+类固醇激素±NK1受体拮抗剂)[1类推荐]d1:5HT3受体拮抗剂(任选一种)多拉司琼 100mg po qd格拉司琼 ①2mg po qd ②0.01mg/kg(最大1mg) iv qd ③ 第一剂化疗药前 24-48h 使用皮肤贴剂(规格为3.1mg/24h)昂丹司琼 ①16-24mg po qd ②8-16mg iv qd帕洛诺司琼 0.25mg iv qd类固醇激素地塞米松 12mg po/iv qd(加或不加)NK1受体拮抗剂(任选一种)阿瑞吡坦 125mg po qd福沙吡坦 150mg iv qd罗拉吡坦 180mg po qd如d1未给予NK1受体拮抗剂:5HT3受体拮抗剂(任选一种)多拉司琼 100mg po qd d2-3格拉司琼①1-2mg po qd /1mg po bid d2-3②0.01mg/kg(最大1mg) iv qd d2-3昂丹司琼①8mg po bid d2-3 ②16mg po qd d2-3 ③ 8-16mg iv qd d2-3或加类固醇激素 地塞米松 8mg po/iv qd d2-3如d1给予了NK1受体拮抗剂:如d1选用阿瑞吡坦:阿瑞吡坦 80mg po qd d2-3+地塞米松 8mg po/iv qd d2-3如d1给予福沙吡坦:d2-3不再使用NK1受体拮抗剂,但使用类固醇激素地塞米松 8mg po/iv qd d2-3如d1给予罗拉吡坦:d2-3不再使用NK1受体拮抗剂,但使用类固醇激素 地塞米松8mg po/iv bid d2-3B.包含奈妥吡坦的方案d1:奈妥吡坦300mg/帕洛诺司琼 0.5mg po qd地塞米松 12mg po/iv qdd2-3:±地塞米松8mg po/iv qdC.包含奥拉西泮的方案d1:奥拉西泮 10mg po qd帕洛诺司琼 0.25mg iv qd地塞米松 20mg iv qdd2-3:奥拉西泮 10mg po qd低度致吐风险化疗药引起的急性或迟发性呕吐的预防方案化疗前开始。多日化疗方案时每日使用下列方案: 地塞米松 8-12mg po/iv qd或者:胃复安 10-20mg po/iv 随后如有需要每6h一次或者:普鲁氯嗪 10mg po/iv 随后如有需要每6h一次或者:5HT3受体拮抗剂(任选一种)多拉司琼 100mg po qd格拉司琼 1-2mg po qd昂丹司琼 8-16mg po qd极微致吐风险化疗药引起的急性或迟发性呕吐的预防方案无需预防呕吐。爆发性呕吐治疗方案治疗爆发性呕吐的原则为:在原预防方案中加一种作用机制不同的药物。 非典型精神类药品奥拉西泮10mg po qd苯二氮平类劳拉西泮 0.5-2mg po/iv q6h大麻素屈大麻酚 5-10mg po q3-6h大麻隆 1-2mg po bid其他氟哌啶醇 0.5-2mg po/iv q4-6h胃复安 10-20mg po/iv q4-6h莨菪碱透皮贴剂 q72h吩噻嗪类普鲁氯嗪 25mg q12h 或者10mg po/iv q6h异丙嗪 25mg po q6h或者12.5-25mg po/iv q4-6h(仅限中心静脉)5HT3受体拮抗剂(任选一种)多拉司琼 100mg po qd格拉司琼①1-2mg po qd ②1mg po bid ③ 0.01mg/kg(最大1mg) iv qd ④第一剂化疗药前24-48h 使用皮肤贴剂(规格为3.1mg/24h)昂丹司琼16mg po/iv qd类固醇激素 地塞米松 12mg po/iv qd若控制有效,则持续有规律的治疗,而不再是有需要时治疗。若控制无效,则重新评估患者情况,可考虑加大止吐药剂量或再加用一种不同作用机制的止吐药。下次化疗前考虑选用提升一个危险级的预防呕吐方案
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科5931人已读 - 典型病例 ”小孔“也能解决大问题
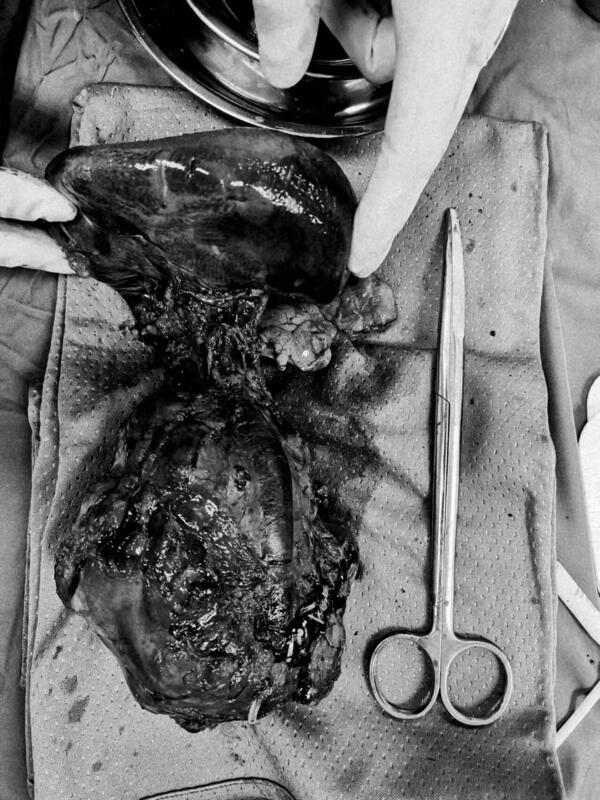
近来,天津医科大学肿瘤医院胰腺肿瘤科高松副主任医师治疗组,为一例胰腺体尾部巨大囊实性占位伴胆囊多发结石的患者成功实施了腹腔镜下脾胰体尾切除术联合胆囊切除术。 患者为68岁老年男性,已发现腹腔内巨大占位(13*10*10cm)3年余,但因为对肿瘤位置不明确及惧怕开刀手术一直对手术切除肿瘤持犹豫态度。在门诊,高松副主任医师针对患者的强化CT做出胰腺体尾部囊腺瘤,胆囊多发结石的明确诊断,并告知患者大爷:“虽然是两个病灶,其中一个还较大,但手术完全可以在腹腔镜下同期进行,一次解决问题!”,患者大爷听到不需要开刀,微创就能解决问题,欣然办理了住院,准备接受手术。 入院后,治疗组对患者的肿瘤再次进行了包括三维重建的强化CT及超声内镜在内的细致检查,明确了肿瘤与脾动静脉,肠系膜上动脉,肠系膜上下静脉及胃左静脉之间的毗邻关系,制订了自右侧胰腺颈部开始游离,逐渐向左侧推进的联合脾脏切除的顺行性切除策略,同时计划术中进行胆囊切除。 手术最终在周密的计划下顺利进行,由高松副主任医师担任主刀,仅用3个小时便在腹腔镜下将13cm的“大块头”胰腺肿瘤联合脾脏一并顺利切除,同时完成了胆囊切除术。手术采取5孔法,两个操作孔置入引流管,脐上开4cm左右切口,取出切除的所有肿瘤标本。术中治疗组对胰腺残端进行了细致的加固缝合,封闭胰管,避免了胰体尾切除术后常见的“胰瘘并发症”,术后2天,患者恢复排气及口入饮食,术后7天患者便顺利出院,病理证实为胰腺多囊性囊腺瘤,胆囊结石伴胆囊息肉。根除了埋藏3年的“定时炸弹”,患者大爷出院时也对借助“小孔”便能完成如此大型肿瘤切除的腹腔镜技术赞不绝口,以为按照传统手术方案要开双侧切口才能切除分居身体两侧的胆囊和胰腺两处病灶。 天津医科大学胰腺肿瘤科高松副主任医师治疗组专注于各类胰腺良恶性肿瘤的微创治疗,希冀为广大有微创要求的患者通过“小孔”手术解决“大问题”。
 高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科655人已读
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科655人已读 - 医学科普 最大程度减轻胰腺肿瘤切除手术的损伤---腹腔镜保留脏器功能的胰腺切除手术
近年来,随着影像学技术的不断进步及广大民众对胰腺相关肿瘤认识的逐渐加深,越来越多的低度恶性或者良性胰腺肿瘤在日常查体时被发现,例如:胰腺囊腺瘤,低级别神经内分泌肿瘤,实性假乳头状瘤或直径较小位置局限的导管内乳头状粘液瘤等。按照传统开放手术治疗理念,上述肿瘤的切除范围与恶性肿瘤相差无几,也需要做胰腺联合周围脏器的大范围切除,这类的手术往往对患者的生存质量,尤其是进食习惯产生了较大的影像,也让这类患者对就医望而却步,选择保守观察,但其中一部分需要手术治疗的患者往往错失手术机会,观察的过程中发现了远处转移或肿瘤复发。 随着腹腔镜手术近十年来的加速开展,腹腔镜下保留胰腺周围脏器功能和结构的胰腺切除术逐渐成为低度恶性肿瘤的首选术式,该类手术具有创伤小,保留必要的脏器结构和功能,恢复快,术后生活质量高等特点。例如生长的胰腺体尾部的低度恶性肿瘤,我们能够在保证切缘和根治度的前提下,施行保留脾脏的胰体尾切除(传统开放手术多行脾胰体尾切除)或者胰腺中段切除术联合胰肠吻合术;位于胰头的肿瘤,可以施行保留十二指肠的胰头切除术(传统开放手术多行胰十二指肠切除术:联合胃胆胰肠的联合切除术还要重构消化道);对于更局限的胰腺肿瘤,我们甚至可以实施胰腺肿瘤局部剜除术和胰管修补术。当然,保留脏器功能的前提还是要根治肿瘤,因次保留脏器功能的腹腔镜胰腺切除术也都是有一定的手术指征的,比如术前影像学明确诊断为低度恶性肿瘤且术中切缘保证阴性(切除量足够),肿瘤与周围脏器重要供血血管无明显侵犯,肿瘤周围无明显淋巴结转移或其他侵犯周围组织证据,腹腔镜下可行安全切除,无重大切除手术风险。 本人目前就职与天津市肿瘤医院胰腺肿瘤科,专注于开展腹腔镜下保留脏器功能的胰腺手术,目前能够顺利开展腹腔镜下保留脾脏的胰体尾切除,胰腺中段切除,保留十二指肠的胰头切除,胰腺肿瘤剜除等手术,最小手术患者年龄12岁,年龄最大患者73岁,术后平均住院时间8.4天。请有需要的患者来我院门诊找我就诊。 本人门诊为每周二下午1:30-4:00,每周五上午8:30-12:00.
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科507人已读 - 医学科普 卡氏评分的普及
体力状况评分标准(KPS评分)依据病人能否正常活动、病情、生活自理程度,把病人的健康状况视为总分100分,10分一个等级。见下表: 健康状况自我评分标准(KPS评分标准) 100身体正常,无任何不适 90 能进行正常活动,有轻微不适 80 勉强可进行正常活动,有一些不适 70 生活可自理,但不能维持正常生活或工作 60 有时需人扶助,但大多数时间可自理 50 常需人照料 40 生活不能自理,需特别照顾 30 生活严重不能自理 20 病重,需住院积极支持治疗 10 病危,临近死亡 0 死亡 得分越高,健康状况越好,越能忍受治疗给身体带来的副作用,因而也就有可能接受彻底的治疗。得分越低,健康状况越差,若低于60分,许多有效的抗肿瘤治疗即无法实施。
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科9417人已读 - 媒体报道 腹腔镜超声应用于胰腺癌分期
随着腹腔镜技术的普及和深入,人们越来越关注腹腔镜手术中因触觉丧失又无法直视的腹腔内脏器深部及腹膜后间隙的病变,病灶与邻近器官之间的解剖关系等问题。腹腔镜超声(Laparoscopic ultrasonography, LUS)的问世使腹腔镜外科如虎添翼,治疗范围也更广泛,几乎涉足了开腹手术的各个领域。 近年来,利用LUS对胰腺癌进行诊断和分期,肿瘤侵犯程度或淋巴结转移做出进一步评估,选择适宜的手术方法,使病人最佳临终前的生活质量的方法引起了国内外学者的高度重视。 1、戳孔的位置 Machi则主张采用三孔法,即经剑突下、右肋缘下、脐部戳孔置入探头,他认为两孔法难以同时做到对肝脏和胰腺的全面扫描[7]。由于胰腺属腹膜后器官,显露不易,常常需要辅助性手术器械在镜下以适当的动作将阻挡在胰腺前面的胃肠道、大网膜推开,或分离胃结肠韧带以进入小网膜囊,三孔法有利于置入显露与分离用辅助性手术器械。胰头部的扫描最好经剑突下戳孔完成,而胰体尾的扫描则通过右侧腹壁或脐部戳孔较佳。值得注意的是,估计已无法行根治性切除,拟行腹腔镜下的胆道内引流术时,戳孔的位置应与四孔法腹腔镜胆囊切除(LC)所需相同。 2、腹腔镜检查 Cuschicri 1999年首先将腹腔镜技术应用于胰腺癌的诊断及临床分期,其目的是发现腹膜后肿大淋巴结及肝脏转移结节,减少不必要的剖腹探查。Sban-Kettering癌肿中心应用多孔腹腔镜进行胰腺癌的诊断与分期,其操作如剖腹探查一样,先评估原发灶,检查肝脏和肝门,切开网膜,检查肝尾叶、腔静脉、腹腔动脉和小网膜囊,确定Traitz氏韧带,观察结肠系膜、十二指肠和空肠。在下列腹腔镜检查结果才能判定肿瘤不能切除:(1)肿瘤向胰外扩展,如横结肠系膜;(2)腹腔动脉或门静脉淋巴结已被侵犯;(3)肿瘤已包绕腹腔动脉或肝动脉;(4)肿瘤已包绕门静脉、肠系膜上动、静脉。 如发现有腹膜的多发性种植、肝脾表面的转移灶、胃十二指肠或横结肠系膜广泛的直接侵犯,特别是根治手术切除范围以外的侵犯,提示已无根治性切除的可能性。如腹腔镜下的病变不能确定为转移灶,且此转移灶在规定的切除范围之外,应在镜下行活检术。Collen等提出扩展腹腔镜分期术,通过腹腔四个方位的系统检查,明确有无转移灶。在腹腔镜下行腹腔灌洗并收集灌洗液行细胞学检查,可判断有无肿瘤细胞的脱落种植性转移。腹腔灌洗液中癌细胞的阳性发现,预示着肿瘤已不可根治性切除。若腔镜检查未发现根治性手术的禁忌,即行LUS检查,做进一步的分期。 3、腹腔镜术中超声扫描 鉴于腹腔镜的分期受到下列限制:(1)仅是二维检查;(2)不能手指触摸;(3)不能正确评估肿瘤与腹膜后血管的真正关系。经腹腔镜超声扫描有助于解决这些问题,尤其是肝实质内的微转移灶。Machi推荐:在需同时扫描肝、胰的情况下,先经右侧腹壁戳孔置入超声探头,可一次完成大部分的肝胰扫描而不需做探头的换位。 一般腹腔镜术中超声检查胰头和钩突部时,可将探头直接置于欲扫描部位,即胃结肠韧带表面,也可采用经十二指肠第一、二段的前外侧作为超声窗扫描。胰头癌扫描的重点在胰头部,目的是了解有无癌肿对肠系膜上动静脉及下腔静脉的直接侵犯,而肠系膜上血管的受侵,是导致胰头癌丧失根治性切除机会最主要的原因。打开多普勒血流显像开关,可良好地显示出肿块与门静脉、肠系膜上静脉、肠系膜上动脉、下腔静脉、腹主动脉等重要的胰周大血管的关系。胰体尾癌容易转移至脾脏,扫描脾脏时探头应自右侧腹壁戳孔或脐部戳孔置入,检查胰体尾部时,采用经胃前壁的超声窗效果较佳。 LUS在检出术前影像检查未能发现的肝脏深部的微小转移灶方面具有无可争议的优越性。一旦确定肝内有多发的术前影像检查未发现的转移灶,即已无必要再行无意义的剖腹探查。
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科3758人已读 - 医学科普 发泡饮料会增加患胰腺癌风险
Karolinska Institutet一项新的研究报道,甜味食品和饲料的大量消耗增加了患胰腺癌的危险。大量食用发泡饮料、奶油水果和咖啡加糖是增加这种危险的三种最常见的方式。 由于葡萄糖代谢紊乱,胰腺产生更高水平的胰岛素,胰腺癌是可能由此导致的非常严重的一种癌症。众所周知的增加胰岛素分泌的办法就是吃很多糖。科学家们现在首次表示,食用加糖的食物和饲料影响了人患胰腺癌的机率。 这项研究在1997年开始,科学家们调查了80,000个健康的男性和女性的饮食,并一直监测到了2005年6月。根据癌症的登记情况,这组人群中有131个人患了胰腺癌。研究者们现在能够推断患胰腺癌与食物中的糖分有关。最危险的是那些饮用大量发泡或含糖浆饮料的人。这组人群中,那些每天饮用2次或更多此类饮料的人比那些从不饮用此类饮料的人高出90%的危险。每天至少5次在食物或饮料(咖啡)中加糖的人比那些从不加糖的高出70%的风险。每天至少一次吃奶油水果(类似松软果酱的食品)的人也有着更高的发病危险。他们患胰腺癌的危险比那些从不吃奶油水果的人高出50%。
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科1578人已读 - 学术前沿 齿龈疾病与男性胰腺癌相关
美国研究人员发现,口腔卫生不良造成的齿龈疾病与男性胰腺癌有关。 研究带头人、哈佛公共卫生学院Dominique Michaud博士称,他们的研究第一次有力证实,牙周疾病可以增加胰腺癌危险性。研究发表于最新一期《国立卫生研究所杂志》。Minaud博士及其同事研究了保健专业随访研究(HPFS)收集的51000人的健康相关资料。结果表明,有牙周病病史的男性胰腺癌发病风险比无此病史的男性高64%。严重牙周炎,如近期伴牙齿脱落者危险性更高。未发现其他口腔卫生疾病如牙齿腐烂与胰腺癌有明确相关。 早先其他研究发现牙齿脱落或牙周炎与胰腺癌有关,即牙周病患者血液中炎性标志如C反应蛋白(CRP)增高。CRP是免疫系统对持续炎症的早期反应性标志之一,与胰腺癌发生有关。在本研究中,研究人员发现,牙周病患者口腔中存在的致癌物质与可能胰腺癌发病风险有关。这种致癌物质(亚硝胺)及细菌与消化道中的消化物质反应,使肠道环境有利于胰腺癌的发生。此研究的意义在于,它强调了良好的口腔卫生不仅可以保持口腔健康,同时还可以减少胰腺癌发病因素。牙周炎、牙龈炎是两种常见口腔感染。牙龈炎是牙齿周围软组织感染,持续的牙龈炎将导致牙周炎。牙周炎侵犯牙齿支持组织,也与牙槽骨吸收有关。约半数30岁以上的美国人患有牙周炎。食物残渣、唾液及矿物质逐渐堆积,在牙根部形成菌斑,细菌即在此增生。菌斑变硬增厚,即形成所谓的牙垢或牙石,它是一层很硬的钙化层,一般不能通过刷牙去除,必须牙医处理。牙石还会沉入牙龈中牙齿根部周围的牙袋内。如此为细菌提供了理想的增生环境并导致牙龈炎症。大多数人症状轻微,口臭、有少量出血,很少有疼痛或刺激性症状,故早期不易诊断。
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科1441人已读 - 医学科普 血管置换技术显著提高胰腺癌的根治性手术切除率
近年来随着社会经济的发展和人们生活水平的提高,胰腺癌的发病率呈显著增加的趋势。但胰腺癌恶性程度高、生物学行为差。肿瘤早期患者症状体征不明显,故一旦发现多为晚期,失去根治性手术机会,手术切除率仅为20-30%。 胰腺癌患者失去手术机会的主要原因有:1)出现远处转移,如肝脏转移、腹腔转移等。2)肿瘤局部进展,累犯胰腺周围的重要血管,导致肿瘤无法完整切除。因此提高胰腺癌根治性手术切除率,对于改善患者预后,延长患者生存期有重要的临床意义。要提高胰腺癌手术切除率,除了对胰腺癌进行早期发现,早期诊断以外,加强对局部进展肿瘤的治疗在一定程度上也起到重要作用。 局部进展的胰腺癌,肿瘤如果累犯的是动脉,则提示肿瘤易出现后腹膜的转移,不易行根治性肿瘤切除,仅可行姑息性的手术治疗。但对于单纯静脉受累的患者,采用先进的血管置换技术可使传统概念上无法切除的肿瘤到达完整切除的目的,从而有效的提高了胰腺癌根治性切除率。 我院胰腺肿瘤科已成功的为多名局部进展期胰腺癌患者施行了血管置换手术,对于静脉累及范围小于5cm者,我们采用原位血管切除+局部重建对端吻合,对于静脉累及范围超过5cm者,我们使用采用人工血管替代受累的病变静脉,使原本无法完整切除的肿瘤得到了根治切除,从而提高了胰腺癌根治性手术的比例。该手术风险低,术后并发症少,收到了良好的治疗效果。 目前,我们已经为10余例患者进行了血管局部切除重建或人工血管置换术,术后患者恢复良好,患者最长生存期4年,目前仍存活。
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科2494人已读 - 医学科普 胰腺导管内乳头状粘液肿瘤特点
胰腺导管内乳头状粘液性肿瘤是最近几年被认识的一种胰腺囊性肿瘤。对该肿瘤曾有不同的命名,如产粘液癌、高分泌粘液癌、导管内乳头状肿瘤、导管高分泌粘液肿瘤、导管内癌、导管产粘液肿瘤、导管扩展型粘液性囊腺瘤和囊腺癌、粘液性导管扩展症、胰管扩展型产粘液肿瘤、胰腺导管内乳头状粘液性肿瘤。国际胰腺癌研究组、WHO 、美国军队病理研究所及日本胰癌处理规约均将具有胰管上皮乳头状增殖、黏液过度分泌特征或二者其一者统称为IPMT并成为目前国际上广为认同的概念。现在胰腺导管内乳头状粘液性肿瘤是当今被采用的术语,以避免与其他一些胰腺产粘液肿瘤如胰腺粘液性囊性腺瘤或囊腺癌的混淆。 以往由于缺乏分类标准, 对胰腺分泌黏液的囊性肿瘤的认识较混乱。1996 年,WHO 分类方法明确了对IPMT 的组织学分类, 从组织学上将其分为良性( 导管内乳头状黏液瘤) 、交界性( 有中度不典型增生的导管内乳头状黏液性腺瘤) 和恶性( 导管内乳头状黏液癌) 三类。目前所采用的IPMT 的命名, 旨在避免与其他一些胰腺分泌黏液的肿瘤如胰腺黏液性囊腺瘤(mucinous cystic tumor of the pancreas,MCT)相混淆。IPMT 倾向于胰腺导管内播散,而且扩张的胰管由乳头状肿瘤上皮覆盖。根据肿瘤的起源不同, 通常将IPMT 分为3 种类型: ①主胰管型: 主胰管扩张且肿瘤主要存在于主胰管; ②分支胰管型: 分支胰管扩张, 肿瘤不存在于主胰管; ③混合型: 肿瘤既存在于主胰管又存在于分支胰管。目前研究表明IPMT 与MCT 有以下共同点: ①两种肿瘤均起源于胰管上皮; ②均产生大量黏蛋白; ③均常见乳头突起这一病理特征。而IPMT 的临床特征包括: ①胰腺导管内大量的黏液产生和潴留; ②乏特乳头部开口由于黏液流过而扩大; ③主要在主胰管内发展和播散; ④很少有浸润性倾向; ⑤手术切除率高及预后良好。Sugiura报道,大部分IPMT中伴有慢性胰腺炎的病理学改变, 至少为局限性间质纤维化和外分泌腺萎缩。IPMT 的基本病理改变是胰管内分泌黏液的异常上皮导致胰管内大量黏液潴留、胰液淤滞和胰管扩张, 这种病变可沿胰管表面扩展形成扁平损害, 也可排列形成微乳头或巨乳头样病变突入胰管腔。IPMT 的病理改变呈多样性, 包括增生、腺瘤、不典型增生、原位癌、浸润癌等; 组织学上增生上皮体积常超过正常细胞的2倍, 并由非乳头状增生向乳头状增生过渡。这些改变提示IPMT 包括从非乳头状和乳头状增生经腺瘤发展为腺癌的演变过程。而MCT 组织学上绝大多数有卵巢样基质( ovarian-type stroma) , 影像学常呈圆形, 有共同的包膜, 多无主胰管扩张, 周围完全由纤维组织包围, 多见于中年女性以及胰体尾部。然而, 少数IPMT 与MCT 在病理学诊断方面仍存在较大困难。 该病常见老年人, 最多见于60~70 岁, 男: 女约2: 1。一般认为, IPMT 早期无特异性临床表现,可出现腹痛、腰背部疼痛、消瘦、黄疸、腹泻等。Kimura 等总结日本、欧洲、美国等地259 例IPMT病人资料, 发现有上腹痛症状者占51.8%, 乏力、纳差者占13.0%, 消瘦者占11.4%, 此外也有少部分病人可出现黄疸, 但其发生率远低于一般的胰腺癌。等报道43 例IPMT 病人中有临床症状者占23 例,其中腹痛12 例,腰背部疼痛5 例,体重下降、糖尿病及淀粉酶升高各2 例, 高达58.6%的病人曾有胰腺炎发作病史, 这可能是由于胰管内大量黏液积聚, 导致胰管内高压, 使小腺泡破裂, 胰液外溢造成胰酶激活, 从而引起了胰腺炎反复发作。此外,41.4%的病人合并糖尿病。因此, 临床上对于胰腺炎反复发作以及合并糖尿病的病人应提高警惕, 防止发生误诊与漏诊。 IPMT患者具有一定的家族遗传倾向并常伴发其它器官恶性肿瘤,有报道IPMT患者伴发其它器官恶性肿瘤高达35%,提示与IPMT发生相关的基因值得进一步研究。 在CT影像上主要表现为葡萄串样或分叶状囊性病灶堆聚,同时伴有胰管的明显扩张,病灶与胰管相通,通常病灶实性成分不易显示, 表现为结节状类圆型软组织影, 由较小囊性病变融合而成。平扫均为低密度影, 增强后边界稍有强化,并伴有不同程度的全程胰管扩张, 伴有假乳头形成,但如发现较明显的实性结节,应考虑恶性IPMN。发生于胰腺的囊性肿瘤及肿瘤样病变相对较多,鉴别有一定困难,IPMN 与其他胰腺囊性肿瘤的主要区别点之一是IPMN 的囊样病灶与扩张的胰管是相通的,而其他胰腺囊性肿瘤与胰管是不相通的。 MRI 可显示主胰管型T2WI 表现为高信号扩张的主胰管,有弥漫扩张,节段扩张,部分可见等信号的壁结节,平均直径约1cm(015 cm~2 cm) 。分枝型表现为葡萄串状或单个的长T1 长T2 信号肿瘤,平均直径6 cm(2 cm~9 cm) ,部分内有壁结节,平均直径约2 cm(1 cm~4cm) 。往往伴有胰腺有不同程度的萎缩和例钙化,或伴主胰管扩张。增强MRI 显示壁结节明显强化。还可清楚地显示分枝型和主胰管之间的交通。 ERCP 显示大乳头肿大,流出粘液,局部或弥漫主胰管扩张和分枝胰管囊状扩张,及由于壁结节的存在所至的充盈缺损。此外还可利用ERCP ,在超生引导下抽取囊和胰管内液体进行诊断。对于难以与胰腺癌或慢性胰腺炎相鉴别的病例, ERCP检查可作为金标准,经口胰管镜检查可观察到主胰管内呈息肉样肿物或胰管黏膜呈绒毛状改变。胰管内超声( IDUS)操作复杂,尚未普及。但资料显示, IDUS对结节状病变的检出率、发现多发病变及定性诊断率均高于超声内镜(EUS)。 IPMT 极易被误诊::临床症状缺乏明显特征性, 其导管扩张程度以及产生黏液量决定其临床症状和体征。(1)IPMT 在临床症状和实验室检查方面无特异性, 因此在诊断上主要依靠影像学及术后病理诊断。(2)当CT 显示胰腺肿块为分叶状或结节状囊性病灶伴有胰管扩张即应考虑诊断本病。有条件者可做ERCP 检查, 如发现十二指肠乳头增大, 胰管显著异常扩张和黏液溢出, 即可临床诊断。 由于IPMT 与胰腺导管癌有着截然不同的生物学行为和预后, 治疗原则也有所不同。IPMT 一旦诊断明确, 手术切除是首选的治疗方式。然而, 目前对IPMT 术前良恶性的判断、肿瘤侵犯的范围及程度的确定等还有一定困难, 因此对手术方法的选择仍有争议。一般认为, 术前考虑为良性的IPMT 倾向于保留胰腺和胃肠功能的手术方案, 包括保留幽门的胰十二指肠切除术( PPPD) 、保留十二指肠胰头切除术、胰腺钩突局部切除术、胰腺节段性切除术、保留脾脏的胰体尾切除术等。如在术前或术中发现IPMT 病变有沿胰管扩展的趋势, 可根据术中冷冻切片确定切除范围, 以确保切缘阴性。对于交界性IPMT 或非浸润性恶性IPMT, 可行胰腺部分切除术。对恶变者,可发生淋巴结转移、神经侵犯, 因此对浸润性癌需行胰十二指肠切除、全胰切除或胰体尾切除以及区域淋巴结清扫术, 以减少术后肿瘤复发率。由于全胰切除术对病人有较大的创伤, 并严重影响术后生活质量, 一般仅用于全胰胰管病变的病人。如术中估计追加切除有危险, 且断端仅有异型增生而并无浸润癌者可行部分切除, 术后密切随访有无复发情况。十二指肠乳头成形术有助于黏液排出, 可缓解症状, 但仅限于不能耐受胰腺切除术的病例。由于其与胰腺导管腺癌在生物学行为及预后等方面有着较大差别, 因此对IPMT 的
高松 副主任医师 天津医科大学肿瘤医院 胰腺肿瘤科1.1万人已读





